. |
||
Treibhauseffekte
Der heutzutage negativ belastete Treibhauseffekt
wird schon seit
Jahrtausenden in der passiven
solaren Architektur angewandt. Ein
Glashaus bzw. Wintergarten wird seit
Jahrhunderten als "Sonnenfalle" genutzt.
Im 16. Jahrhundert wurden ein Glashaus
als Gewächshaus (Orangerie) zur
Aufzucht von Pflanzen verwendet. Aber der gleiche Effekt führt zunehmend
zur Erderwärmung.
Verantwortlich sind die in der Atmosphäre vorhanden bzw. eingetragenen Gase (Treibhausgase - Klimagase) bezeichnet. Aber hier beginnt der Streit, welche Faktoren und Vorgänge wirklich für die Erderwärmung ausschlaggebend sind.
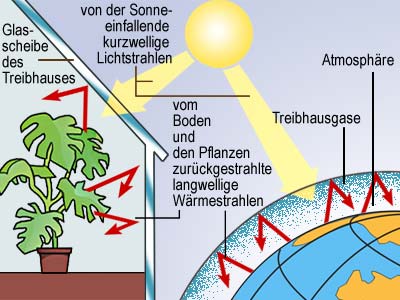
Um das Phänomen der Erderwärmung einfach zu erklären, werden die Vorgänge innerhalb eines Treibhauses herangezogen. Hier wird die Sonnenstrahlung durch die Glasscheiben durchgelassen, aber die Erwärmung der internen Flächen nicht wieder herausgelassen.
Der Streit, welche Gase (Klimagase, auch Treihausgase genannt) in der Atmosphäre naturgegeben (atmosphärischer Treibhauseffekt*1) oder von Menschen verursacht (anthropogener Treibhauseffekt*2) sind, wird wohl ständig weitergeführt. Letztendlich sind viele verschiedene Gase für den Klimawandel (Erderwärmung) verantwortlich. Alle diese Gase kommen in einem mehr oder weniger großen Anteil in der Natur vor.
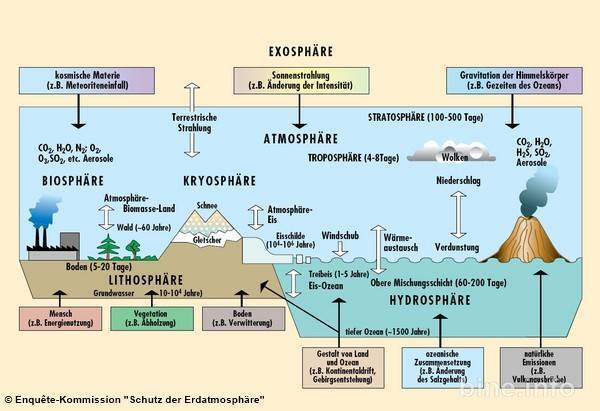
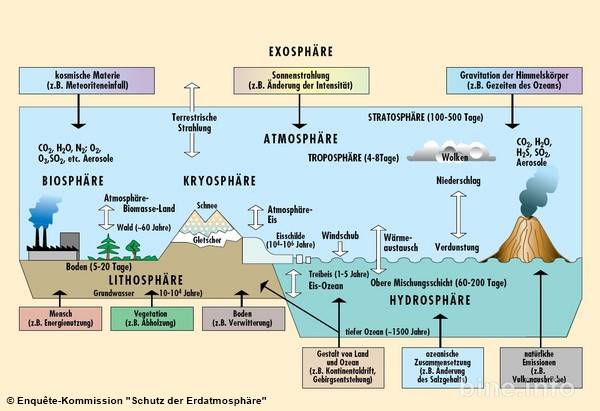
*1 Die Sonne beeinflusst das Klima der Erde, indem sie in sehr kurzen Wellenlängen Energie ausstrahlt (überwiegend im sichtbaren oder fast sichtbaren [z. B. ultravioletten] Teil des Lichtspektrums). Ein Drittel der Sonnenenergie, die die Oberfläche der Erdatmosphäre erreicht, wird direkt zurück ins All reflektiert. Der Rest wird von der Erdoberfläche und in geringerem Umfang auch von der Atmosphäre absorbiert. Um die absorbierte Energie auszugleichen, muss die Erde durchschnittlich dieselbe Energiemenge wieder ins All zurückstrahlen. Da die Erde viel kälter ist als die Sonne, strahlt sie in viel längeren Wellenlängen, vorwiegend im infraroten Teil des Lichtspektrums. Ein Großteil dieser von Land und Ozean abgegebenen thermischen Strahlung wird von der Atmosphäre einschließlich der Wolken absorbiert und zur Erde zurückgestrahlt.
*2 Freisetzung klimawirksamer Spurengase (Klima- bzw. Treibhausgase), Partikelemissionen Ruß, Feinstaub, Staub bzw. Sandkörner) und Veränderungen der Erdoberflächenbeschaffenheit (städtische Siedlungsgebiete, Landtrockenlegung, Waldrodung)
- Wie wirkt sich die gleichzeitige Absorption und Emission von Wärmestrahlung in den verschiedenen Höhen der Atmosphäre aus?
- Wie wirken sich die Strömungen in der Atmosphäre aus?
- Haben die Vorgänge einen größeren anthropogenen (menschlichen) Einfluss oder sind es natürliche Vorgänge?
- Welchen Einfluss haben die vermehrte Wolkenbildung und der Aerosolausstoß der Vulkane?
- Wirken diese Vorgänge ausgleichend?
Klimawandel und Treibhauseffekt - Berliner Wasserbetriebe
Zusammenhänge und Wechselwirkungen im Klimasystem - Jucundus Jacobeit
Biosphäre im Klimasystem - Bildungsserver
Neue Wälder als Klimaretter?
Moore: Die vergessenen CO2-Speicher
Mit Algenfarmen das Klima retten
Der Treibhauseffekt wird schon seit Jahrtausenden in der passiven solaren Architektur angewandt. Ein Beispiel ist das antike Griechenland vor rund 2.500 Jahren, das damals ebenfalls in einer Energiekrise steckte. Als Lösung für das Problem des immer knapper und teurer werdende Brennholzes wurde die verglaste Südfläche mit weitüberstehendem Vorbau entwickelt. Sokrates beschrieb dies so: "In Häuser, die nach Süden blicken, dringt die Sonne im Winter durch die Vorhalle bis in die Wohnräume vor und wärmt sie. Im Sommer jedoch hält das Dach der Vorhalle die Sonne ab und spendet kühlenden Schatten." mehr > hier ein paar Beispiele Quelle: Buch der Synergie - Achmed A. W. Khammas
Ein Glashaus bzw. Wintergarten wird seit Jahrhunderten als "Sonnenfalle" genutzt. Im 16. Jahrhundert wurden ein Glashaus als Gewächshaus (Orangerie) zur Aufzucht von Pflanzen verwendet. Diese überdachten botanischen Gärten wurden freistehend oder an die Häuser gebaut. In der heutigen Zeit gehört ein Wintergarten durch die Entwicklung der Glasherstellung und der technischen Weiterentwicklung der Lüftungstechnik schon zu der "normalen" Ausstattung im gehobenen Wohnungsbau. Hier wird er hauptsächlich zu der Erweiterung der Wohnfläche verwendet und hat als Nebeneffekt die Nutzung der Sonnenenergie.
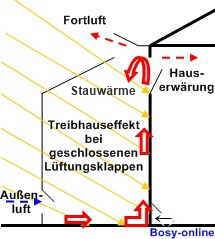
In jedem Glashaus
und Wintergarten
wirkt der "Treibhauseffekt" bzw. "Glashauseffekt".
Das bedeutet, der größte Anteil der Sonnenstrahlung
dringt durch die Glasscheiben, da der Hauptanteil der Sonnenstrahlung
im gelben Wellenlängenbereich (0.5 µm)
liegt, für die die Glasscheiben durchlässig sind. Davon
kommen 60 bis 70 % der auf den Boden bzw. Wände. Diese erwärmten
Flächen strahlen die Wärme im infraroten Wellenlängenbereich
(>3.5 µm) ab und diese Wärmestrahlung
wird von den Glasscheiben reflktiert. Wenn die
Wärmestrahlung im Innern des Raumes die Strahlungsleistung
der einfallenden Strahlung von außen erreicht hat, stellt
sich ein Strahlungsgleichgewicht ein. Die Wärme
bleibt also in dem Raum und hierbei wird die Meinung verteten,
dass dabei nicht die Reflektierung der Scheiben bei der Aufheizung
des Raumes eine Rolle spielt sondern nur die Konvektion
an den warmen Flächen und die durch die
Glasscheiben behinderte Lufbewegung. Dadurch
kann keine Wärme abtransportiert werden. > mehr |
Klimagase
Das Kyoto-Protokoll nennt folgende Treibhausgase: Kohlendioxid (CO2), Methan (CH4), und Lachgas (N2O) sowie die fluorierten Treibhausgase (F-Gase): wasserstoffhaltige Fluorkohlenwasserstoffe (HFKW), perfluorierte Kohlenwasserstoffe (FKW), und Schwefelhexafluorid (SF6). Seit 2015 wird Stickstofftrifluorid (NF3) zusätzlich einbezogen.
In Deutschland entfallen 87,1 % der Freisetzung von Treibhausgasen auf Kohlendioxid, 6,5 % auf Methan, 4,6 % auf Lachgas und rund 1,7 % auf die F-Gase (im Jahr 2020). Die Emissionen von Stickstofftrifluorid sind verschwindend gering.
|
Der Streit, welche
Gase (Klimagase, auch Treibhausgase
genannt) in der Atmosphäre naturgegeben (atmosphärisch)
oder von Menschen verursacht (anthropogen) sind,
wird wohl ständig weitergeführt. Letztendlich sind viele
verschiedene Gase für den Klimawandel (Erderwärmung)
verantwortlich. Alle diese Gase kommen in einem mehr oder weniger
großen Anteil in der Natur vor. |
- Kohlendioxid (CO2) > Kohlenstoffdioxid
- Kohlenmonoxid (CO) > Kohlenstoffmonoxid
- Methan (CH4)
- Ozon (O3)
- Distickstoffoxid (N2O) > Lachgas
- Teilhalogenisierte Kohlenwasserstoffe (HKFW)
- Halogenierte Fluorkohlenwasserstofe (FCKW)
- Perfluorierte Kohlenwasserstoffe (PFC)
- Schwefelhexafluorid.(SF6)
- Nichtmethanhaltige flüchtige organische Verbindungen (NM VOC)
- Wasserdampf (H2O)
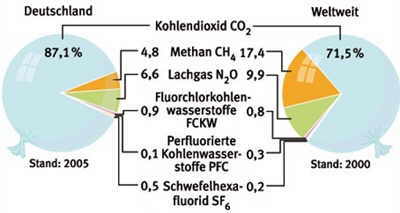 |
Zusammensetzung
der ausgestoßenen Klimagase |
Quelle:
Umweltbundesamt, World Resources Institute, dpa |
Die chemische Formel CO2 steht für Kohlenstoffdioxid. Das Gas ist farb- und geruchslos und weder brennbar noch explosiv oder gesundheitschädlich (kann aber bei einer erhöhten Konzentration gefährlich werden). Es ist gut in Wasser löslich. Die Zusammensetzung von CO2 lässt sich aus seiner Formel ableiten: Es handelt sich um eine Verbindung von einem Kohlenstoffatom (C) und zwei Sauerstoffatomen (O2).
Kohlendioxid bzw. Kohlenstoffdioxid (CO2) ist ein linear aufgebautes Molekül und entsteht durch das Verbrennen fossiler Brennstoffe. Aber auch Menschen emitieren CO2 (ca. 4 % der ausgeatmeten Luft besteht aus Kohlendioxid. So reichert sich der CO2-Gehalt der Raumluft nach und nach an), Tiere und sogar Bäume und Pflanzen emitieren CO2 (durch das Absterben tierischer und pflanzlicher Organismen sowie beim Reifen von Obst und Gemüse) in die Atmosphäre. Kohlendioxid ist ein Klimagas, dass durch die Anreicherung in der Atmosphäre die Wärmeabstrahlung der Erdoberfläche in das Weltall verhindert und so zu einer Erderwärmung über den Treibhauseffekt zum Klimawandel beiträgt.
Auf der anderen Seite spielt Kohlendioxid eine besonders wichtige Rolle bei der Fotosynthese. Dabei werden CO2 und Wasser (H2O )mithilfe von Lichtenergie in Biomasse umgewandelt und es entsteht der für uns lebenswichtige Sauerstoff. Außerdem würde ohne einen bestimmtem Anteil Kohlendioxid (ca 0,038 %) in der Atmosphäre die Wärmestrahlung einfach in das Weltall abgegeben werden und es wäre auf der Erde sehr kalt. CO2 bilden mit der Atmosphäre jedoch eine Hülle und strahlen die Wärme nicht nur in Richtung Weltraum, sondern auch in Richtung Erdoberfläche ab (Treibhauseffekt).
Bei der Verbrennung von fossilen Brennstoffen (ÖL, Gas, Kohle) wird Kohlenstoff freigesetzt, der in den letzten Jahrmillionen gebunden wurde. Die Atmosphäre reichert sich mit diesem Gas an, weil es nicht in diesen Mengen von der Natur aufgenommen werden kann. Ein Teil dieses Gases wird auch zum großen Teil in den Ozeanen gebunden und senkt den pH-Wert des Wassers.
In festem Aggregatzustand dient Kohlendioxid als Trockeneis in Form von Blöcken oder Pellets. Es kann bis zu -90 °C für Kühlzwecke betragen und erzeugt Erfrierungen. Bei Normaldruck und einer Temperatur von -78,48 °C sublimiert es, d.h. wird wieder gasförmig. Es entsteht ein dichter weißer Nebel, der früher in der Bühnentechnik eingesetzt wurde.
Anwendung von Kohlendioxid auch in völlig unterschiedlichen Bereichen:
• Beim Schweißen wird es in Form eines Zusatzstoffes für Edelgase wie Argon oder Helium als Schutzgas verwendet, um Sauerstoff von der Schmelze zu verdrängen.
• Es fungiert außerdem als Schutzgas für Verpackungen von Lebensmitteln, um sie vor der Reaktion mit dem Sauerstoff fern und somit länger frisch zu halten. Und ebenfalls zum Konservieren von Obst, Getreide und Gemüse findet Kohlendioxid seine Aufgabe.
• In Gewächshäusern wird das Gas als Dünger genutzt. Denn besonders im Winter fehlt den Pflanzen Nachschub an Frischluft, durch den sie mit einem CO2-Mangel zu kämpfen haben. Kohlendioxid bildet nämlich ihre Grundsubstanz.
• Auch beim Transport von explosions- und brandgefährdeten Schüttgütern mit Gas durch einen Über- und Unterdruck wird Kohlenstoffdioxid zur Hilfe genommen.
• Außerdem wird Kohlendioxid als ein Wasserhärtemittel genutzt. Denn zu weiches Wasser wirkt sich auf einige Werkstoffe korrosionsfördernd aus und kann den pH-Wert über den der Trinkwasserverordnung treiben.
• Als medizinisches Gas wird es häufig als Zusatzstoff zur Beatmung und therapeutisch verwendet. Aber auch aus der minimal invasiven Chirurgie zur künstlichen Erweiterung und Stabilisierung von Körperhöhlen ist das Gas nicht mehr wegzudenken. Und ebenfalls als Abführmittel in Form von Zäpfchen. Schlachthöfe nutzen das Gas, um ihre Tiere vor der Schlachtung zu betäuben und in einen Zustand der Bewusstlosigkeit zu versetzen.
• Im flüssigen Zustand, der bei Umgebungsluft unter Druck entsteht, kann es auch als Vereisungs- oder Kühlmittel, so zum Beispiel beim Transport von Organspenden, dienen.
• In der Kunststoffindustrie wird Kohlendioxid als Treibgas für die Verarbeitung von Kunststoffen in vielerlei Verfahren genutzt. So beim Schäumen, beim Kühlen und um Material zu verdrängen.
• Kohlenstoffdioxid löscht Feuer sehr effektiv, da es den Sauerstoff vom Brandherd verdrängt.
• Das Gas dient ebenfalls zur Hochdruckextraktion, so zum Beispiel extrahiert es ätherische Essenzen aus pflanzlichen Produkten oder das Koffein aus dem Kaffee.
• Zum Reinigen und Entfetten kann Kohlendioxid als Lösemittel verwendet werden, so beispielsweise in der Chemischen Reinigung von Textilien.
• In festem Aggregatzustand dient Kohlendioxid als Trockeneis in Form von Blöcken oder Pellets. Es kann bis zu −90 °C für Kühlzwecke betragen und erzeugt Erfrierungen. Bei Normaldruck und einer Temperatur von −78,48 °C sublimiert es, d.h. wird wieder gasförmig. Es entsteht ein dichter weißer Nebel, der früher in der Bühnentechnik eingesetzt wurde.
• Getränken wie Wasser und Limonade wird Kohlendioxid zugeführt, um die prickelnde Kohlensäure, wie sie im Volksmund genannt wird, zu erzeugen. Aber auch für die Wein-, Sekt- und Bierproduktion, ist Kohlendioxid unabdingbar, um den Sauerstoff von den Reben fernzuhalten.
Quelle: GPG Gase Partner GmbH
Kohlenstoffdioxid
chemie.de - LUMITOS AG
Alles Wissenswerte über CO2 verständlich erklärt
Elektro4000 - Hagen E-Commerce GmbH
Kohlendioxid in der Atmosphäre
Rheinland-Pfalz Kompetenzzentrum für Klimawandelfolgen
bei der Forschungsanstalt für Waldökologie und Forstwirtschaft
-Kohlenstoffdioxid (Co2) - das Gas zum Prickeln
GPG Gase Partner GmbH
CO2-Abscheidung und Speicherung
|
Trockeneis ist Kohlenstoffdioxid (Kohlensäure*) in fester Form. Die Bezeichnung "trocken" bezieht sich auf die Eigenschaft direkt zu verdampfen, ohne zu schmelzen, bzw. flüssig zu werden. |
Trockeneis besteht im Gegensatz zu herkömmlichem Eis nicht aus Wasser, sondern aus reinem Kohlendioxid (CO2), das unter hohem Druck verflüssigt und anschließend durch Expansion schockgefroren wird. Aus diesem Grund geht es bei seinem "Auftauen" direkt vom festen in den gasförmigen Zustand über, ohne eine flüssige Phase zu durchlaufen.
Der Druck und die Temperatur bestimmen die Form der Kohlensäur > den gasförmigen, flüssigen oder festen Aggregatzustand. Trockeneis verdampft direkt, ohne zu schmelzen, d.h. flüssig zu werden. Kohlendioxid ist eines der wenigen Gase, das einen festen Zustand annehmen kann. Die Kälteleistung von Trockeneis beträgt bei Erwärmung von –78,5 °C (194,65 K) auf 0 °C (273,15 K) ca. 640 kJ/kg, dies entspricht etwa der 3-fachen Kühlleistung von herkömmlichem Eis. Der möglicherweise wichtigere Vorteil ist aber, dass nach der Verdampfung nichts mehr übrig bleibt, was bei normalem Eis aus Wasser nicht der Fall ist. Bei Wärmezufuhr geht das Trockeneis sofort in den gasförmigen Zustand über. Es entsteht also keine Flüssigkeit, das Ihrem Kühlerzeugnis oder dessen Verpackung schaden könnte.
Haupteigenschaften
- im gasförmigen Zustand schwerer als Luft
- nicht brennbar
- geht bei Erwärmung vom festen Zustand direkt in die Gasphase über (Sublimation)
- Trockeneis ist tiefkalt (-78,5 °C) und erzeugt Erfrierungen
- nicht giftig, jedoch Wirkung u. a. auf Herzrhythmus und Atemfrequenz; bereits Konzentrationen von 8 - 10 % können nach 30 - 60 Minuten tödlich sein
- erstickend in hohen Konzentrationen
- beim Umgang mit dem Produkt für ausreichende Belüftung sorgen
- Transportkühlung gekühlter und gefrorener Produkte
- Chemische Industrie und Laboratorien: zur Herstellung von Kältebädern, für Kristallisationsprozesse und zur Wärmeabführung bei chemischen Reaktionen, beim Kaltmahlen.
- Metallindustrie zur Materialprüfung: zum Kaltschrumpfen und zum Härten
- Allgemeine Industrieanwendungen: partielle Rohrgefrierung für Revisionszwecke
- Reinigungsverfahren: die "coole" Strahlreinigung mit Trockeneis.
- Unterhaltungsindustrie: Nebeleffekte bei Musicals und in Diskotheken
Trockeneis
LUMITOS AG
Was genau ist Trockeneis? Wir haben die Antwort!
Gernot Schnettler, Dry-Ice-Energy GmbH
Trockeneis was ist das und wozu braucht man es?
SimplyScience Stiftung
Kohlenstoffdioxid (Co2) - das Gas zum Prickeln
GPG Gase Partner GmbH
Welcher Feuerlöscher und warum (Co2)
Georg - akkudoktor.net
 * Kohlenmonoxid
(CO - Kohlenstoffmonoxid) ist nicht nur ein Klimagas sondern auch ein Gas mit höchst
tückischen Eigenschaften, das sehr schnell zu verheerenden Konsequenzen führen kann, wenn es von Bewohnern
eines Hauses oder einer Wohnung nicht bemerkt wird,. CO ist farblos, geruchlos, geschmacklos
und führt zu Vergiftungen. Schon in kleinster Konzentration kann das Gas für den Menschen tödlich sein, wenn
er unbemerkt in den Organismus eintritt. In Häusern und Wohnungen mit Kamin, Kaminofen, Gasherd und/oder raumluftabhängigen und
raumluftunabhängige Wärmererzeuger (Gastherme, Öl, Holz- oder Pelletkessel) sollte ein
CO-Melder vorgeschrieben werden, genauso, wie Rauchmelder heute in den meisten Wohnungen vorgeschrieben sind. Auch sollte man bedenken,
dass von Wärmeerzeugern, die an einem
Luft-Abgas-System
angeschlossen sind und/oder bei denen ein Kondensatsiphon (Brennwerttechnik)
vorhanden ist, die Gefahr besteht, dass Abgase in den Raum austreten können. * Kohlenmonoxid
(CO - Kohlenstoffmonoxid) ist nicht nur ein Klimagas sondern auch ein Gas mit höchst
tückischen Eigenschaften, das sehr schnell zu verheerenden Konsequenzen führen kann, wenn es von Bewohnern
eines Hauses oder einer Wohnung nicht bemerkt wird,. CO ist farblos, geruchlos, geschmacklos
und führt zu Vergiftungen. Schon in kleinster Konzentration kann das Gas für den Menschen tödlich sein, wenn
er unbemerkt in den Organismus eintritt. In Häusern und Wohnungen mit Kamin, Kaminofen, Gasherd und/oder raumluftabhängigen und
raumluftunabhängige Wärmererzeuger (Gastherme, Öl, Holz- oder Pelletkessel) sollte ein
CO-Melder vorgeschrieben werden, genauso, wie Rauchmelder heute in den meisten Wohnungen vorgeschrieben sind. Auch sollte man bedenken,
dass von Wärmeerzeugern, die an einem
Luft-Abgas-System
angeschlossen sind und/oder bei denen ein Kondensatsiphon (Brennwerttechnik)
vorhanden ist, die Gefahr besteht, dass Abgase in den Raum austreten können.Atmet der Mensch eine erhöhte Kohlenmonoxidkonzentration ein, bindet sich das CO direkt an die roten Blutkörperchen (Hämoglobin) und blockiert damit die Aufnahme von Sauerstoff im Blut. Infolgedessen kommt es schnell zu einem Sauerstoffmangel und den damit verbundenen Gesundheitsgefährdungen. Schon geringe Mengen eingeatmeten Kohlenmonoxids führen zu irreversiblen Herz- und Hirnschäden, größere Mengen zum Tod. Die folgende Tabelle beschreibt die Wirkung von Kohlenmonoxid auf den menschlichen Körper in Abhängigkeit zur Konzentration vom Atemgift in der Luft.
|
||||||||||||||||||||||
Der Ozonmangel
in der Stratosphäre (Ozonloch, vor allem über
der Antarktis und Arktis) ist auf den Fluorchlorkohlenwasserstoff (FCKW)
aus Spraydosen und Kältemitteln zurückzuführen. An diesen
Stellen kann die UV-Strahlung der Sonne verstärkt bis zur Erdoberfläche
durchdringen. Das fehlende Ozon hat Auswirkungen auf das Klima und dem
Wachstum der Pflanzen.
![]() Die Hydroxylradikale sind keine klimaschädlichen Gase, aber das wichtigste freie Radikal in der Atmosphäre. Der Abbau der meisten oxidierbaren Spurenstoffe in der Atmosphäre wird durch Reaktion mit OH-Radikalen eingeleitet. Die OH-Radikale werden auch als das "Waschmittel" der Atmosphäre bezeichnet.
Die Hydroxylradikale sind keine klimaschädlichen Gase, aber das wichtigste freie Radikal in der Atmosphäre. Der Abbau der meisten oxidierbaren Spurenstoffe in der Atmosphäre wird durch Reaktion mit OH-Radikalen eingeleitet. Die OH-Radikale werden auch als das "Waschmittel" der Atmosphäre bezeichnet.
OH-Produktion:
• Die wichtigste Quelle der OH-Radikale ist die Photolyse von Ozon durch Licht.
• Eine wesentliche Quelle für OH-Radikale ist auch die Reaktion von HO2-Radikalen mit NO. Allerdings entstehen HO2-Radikale (zumindest in Reinluft) zu einem großen Teil durch Reaktionen von OH-Radikalen.
• Eine weitere OH-Quelle ist die Photolyse von HONO (Salpetrige Säure): Diese OH-Quelle ist aber nur in verschmutzter Luft von Bedeutung wo sich HONO durch heterogene Reaktionen (d.h. Reaktionen an Oberflächen, z.B. von Aerosolteilchen) bildet.
• Auch die Photolyse von Wasserstoffperoxyd kann eine
nennenswerte Quelle von OH Radikale darstellen.
Quelle: Dr. R. Tuckermann, Atmosphärenchemie
Chemie der Troposphäre - Dr. R. Tuckermann, Atmosphärenchemie
Peroxy-Radikale - "Waschmittel" der Atmosphäre - Deutscher Wetterdienst
Ammoniak (NH3)
ist eine gasförmige Verbindung des Stickstoffs (N). Der Luftschadstoff entsteht hauptsächlich
durch landwirtschaftliche Prozesse (z. B. Tierhaltung). Es reagiert in der Atmosphäre mit anderen Gasen zu
gesundheitswirksamen Partikeln (sekundär gebildeter Feinstaub) oder lagert
sich in Ökosystemen ab, wo es auf Pflanzen bzw. das Nährstoffgefüge des Bodens negative Wirkungen
ausüben kann oder in die Stickstoffkaskade (Sequenz von Wirkungen des reaktiven [anthropogen verursachten]
Stickstoffs im biogeochemischen Kreislauf) eintritt.
Aus der Landwirtschaft in Deutschland kommen ca. 95 % des Luftschadstoffs
Ammoniak. Die Ammoniak-Emissionen kommen aus der Rinderhaltung (52 %), der Schweinehaltung (20 %), der Geflügelhaltung (9 %) und der Mineraldüngeranwendung (15 %). Der Großteil der Emissionen In der Schweinehaltung entstehen direkt im Stall und in der
Rinderhaltung bei der Wirtschaftsdüngerlagerung und -ausbringung. Neben Ammoniak werden in der Tierproduktion auch ekelhafte Gerüche und Stäube, die auch biologische Komponenten (z. B Keime) enthalten) freigesetzt.
Durch das Ammoniak und das nach Umwandlung entstehende Ammonium werden die
Land- und Wasserökosysteme erheblich durch Versauerung und Eutrophierung (Nährstoffanreicherung)
geschädigt. Bodenversauerung und Nährstoffüberversorgung natürlicher und naturnaher
Ökosysteme (z. B Moore, Magerstandorte, Gewässer) durch reaktiven Stickstoff können zu Veränderungen der
Artenvielfalt führen. Besonders hohe Ammoniakkonzentrationen in der Umgebung von großen Tierhaltungsanlagen können zu direkten
Schäden an der Vegetation führen. Ammoniak kann sich über die Stickstoffkaskade auch in
eine der zahlreichen anderen umweltwirksamen stickstoffhaltigen Verbindungen umwandeln, mit negativen Folgen
für die Qualität der Atemluft (Bildung von Feinstaub und Ozon), die Wasserqualität (Nitrat in Grundwasser) und
die Verschärfung des Klimawandels (Lachgas).
Für die Ammoniakkonzentration in der Luft gibt es derzeit keine ausreichende Regelung.
Zu viel giftiges Ammoniak in der Luft
Ammoniak - Geruch und Staub
Distickstoffoxid (Lachgas) entsteht bei der Verbrennung von Biomasse (Holz, Stroh, Biogas), durch den Straßenverkehr und in der Landwirtschaft durch den Einsatz von Stickstoffdünger. Es reichert sich in der Atmosphäre an, da es eine Lebensdauer von ca. 150 Jahren hat.
Die Hauptquellen für Lachgas sind stickstoffhaltige Düngemittel in der Landwirtschaft und die Tierhaltung, Prozesse in der chemischen Industrie sowie Verbrennungsprozesse. Dabei ist zwischen direkten und indirekten Lachgasemissionen zu unterscheiden.
Direkte Lachgasemissionen entstehen in der Landwirtschaft selbst, durch reaktive Stickstoff-(Nr)-Einträge aus organischen und mineralischen Düngemitteln und atmosphärischer N-Deposition sowie Nr in Böden aus Pflanzenreststoffen und biologischer N-Fixierung von Eiweißpflanzen (Leguminosen) sind die Grundlage solcher Emissionen.
Indirekte Lachgasemissionen werden verursacht, wenn reaktive Stickstoffverbindungen (Nitrat und Ammoniak) in die umliegenden Naturräume gelangen. Aus reaktiven N-Verbindungen entsteht bei Nitrifikations- und Denitrifikationsvorgängen Lachgas.
Verwendung
Distickstoffmonoxid bzw. Lachgas (N2O) ist ein anorganisches Einstoffkältemittel (R744A). Da Distickstoffmonoxid die gleiche Molmasse wie Kohlendioxid (CO2) aufweist, hat man der kältetechnischen Bezeichnung R744 ein "A" angefügt, um es von Kohlendioxid unterscheiden zu können. Distickstoffmonoxid ist unter Atmosphärenbedingungen ein farbloses Gas, das sich im Temperaturbereich zwischen ca. -90 °C und +36 °C unter entsprechendem Druck verflüssigen lässt. Die Verdampfung kann somit zur Kühlung bis hin zu tiefen Temperaturen genutzt werden.
Wenn Lachgas in der Medizin als Arzneimittel eingesetzt wird, unterliegt es dem Arzneimittelrecht und ist verschreibungspflichtig. Lachgas ist kein Betäubungsmittel im Sinne des Betäubungsmittelgesetzes.
Lachgas wird auch als Treibgas in Spraydosen und als Aufschäummittel in Sahnespenderkapseln gefüllt. In der Industrie wird Lachgas in großem Umfang unter anderem als Laborchemikalie und in der Produktion verwendet. Im Motorsport kommt Lachgas zur Leistungssteigerung zum Einsatz.
Neben der medizinischen Verwendung als Narkosemittel, wobei es zusammen mit Sauerstoff verabreicht wird, wird es auch als Rauschmittel unverdünnt inhaliert. Durch den Sauerstoffmangel droht Bewusstlosigkeit. Konsumierende können dabei stürzen und sich verletzten.
Als Schnüffelstoff eingeatmet, tritt nach wenigen Sekunden ein Rausch ein, bei dem schwache Halluzinationen, Wärme- und Glücksgefühle empfunden werden. Konsumierende berichten von einem traumähnlichen Zustand, in dem sie Raum und Zeit verändert wahrnehmen. Der Rauschzustand hält allerdings nur wenige Minuten an. Der Sauerstoffmangel wird vor allem dann gefährlich, wenn Konsumierende die Intensität der Wirkung steigern wollen, beispielsweise indem sie eine mit Lachgas gefüllte Plastiktüte über den Kopf ziehen. Bei Bewusstlosigkeit droht Erstickungsgefahr!
Lachgas und Methan - UBA
R744A, ein (fast) unbekanntes Tieftemperaturkältemittel
Institut für Luft- und Kältetechnik Gemeinnützige Gesellschaft mbH
Lachgas - Bundeszentrale für gesundheitliche Aufklärung (BZgA)
Hype um Lachgas: Legaler Rausch mit Nebenwirkungen - Isabel Handrich, ZDF
Der Einsatz dieser Gase ist seit einigen Jahren verboten und dürfen nur mit einer Ausnahmegenehmigung verwendet werden, so z. B. in der Halbleiter- und Aluminiumherstellung.
Messstellen und Messtechniken für Emissions- und Immissionsmessungen - Umweltbundesamt
Quelle:
© Enquête-Kommission "Schutz der Erdatmosphäre" |
||
| Schadstoffmessung | ||
Schadstoffe zu erfassen und zu bewerten ist für Industrie, Behörden, Städte und Gemeinden, für Kurorte und Privatpersonen gleichermaßen wichtig. Es entstehen Messwerte, die zum einen die Basis für wirtschaftliche Entscheidungen bilden, zum anderen sind sie die Grundlage für mögliche Optimierungen oder für die Sicherheit der Mitarbeiter am Arbeitsplatz. |
||
|
||
Setzen Sie Schadstoffen mit Umweltmessungen und Schadstoffmessungen Grenzen TÜV SÜD AG Schadstoffmessung, Schadstoffanalyse, chemische Analyse, Laboruntersuchung bundesweit, deutschlandweitSchadstoff-Messgeräte Lionda GmbH Wohnraum Schadstoffmessung - Reblu GmbH Schadstoff-Messgeräte - Conrad Electronic SE EMV & Umweltmessgeräte - OCS.tec GmbH & Co. KG Gesetz zum Schutz vor schädlichen Umwelteinwirkungen durch Luftverunreinigungen, Geräusche, Erschütterungen und ähnlicheVorgänge (Bundes-Immissionsschutzgesetz - BImSchG) |
||
CO2-Lüge Sind die Kohlenstoffdioxid-Emissionen, die durch das Verbrennen fossiler Brennstoffe (Heizung, Kraftwerke, Autos, Flugzeuge) oder durch das Emitieren durch Menschen, Tiere und sogar Bäume und Pflanzen in die Atmosphäre eingetragen werden, wirklich für die globale Temperaturerwärmung der Atmosphäre verantwortlich? Auf jeden Fall wird durch die Medien und Regierungen ständig behauptet, dass die CO2-Emissionen durch Menschen die Hauptschuld am Klimawandel haben. Die Folge sind immer schärfere Gesetze (z. B. Energieeinsparungsgesetz [EnEG], BImSchG [VO nach dem Bundes-Immissionsschutzgesetz]) und Verordnungen (z. B. Energieeinsparverordnung [EnEV]) zur CO2-Reduzierung. Dass es Veränderungen in einigen Klimazonen gibt, ist eine Tatsache, aber diese Veränderungen hängen auch von sehr vielen anderen Klimafaktoren ab, die näher betrachtet bzw. berücksichtigt werden sollten. - Ständig steigende
natürliche Produktion von Methan.
Dieses Gas ist 20 bis 30mal schädlicher als CO2. |
||
Ist CO2 wirklich ein Klimakiller? |
||
| CO2-Abscheidung und Speicherung (Carbon-Capture and Storage) | ||
Mit 87 % hat Kohlendioxid (CO2 [Kohlenstoffdioxid]) den größten Anteil der freigesetzten Treibhausgase. Neben der Vermeidung bzw. Verminderung (Energiesparen) des Gasaustoßes wird über verschiedene Abscheide- und Speichermethoden diskutiert und teilweise schon umgesetzt. Ohne das gezielte Abfangen (Carbon-Capture - CO2-Abscheidung [Kohlenstoffabscheidung]) von Kohlendioxid aus Abgasen und/oder der Luft wird der Klimawandel nicht zu stoppen sein. >>>> hier ausführlicher <<<< |
||